Sommaire
- Le GIC A3P Validation du Nettoyage prépare un guide pratique pour l’automne 2017 sur le Chapitre 10 de l’Annexe 15 des GMP Européennes : Présentation & discussion.
- Stratégies de regroupement des nettoyages pour les formes orales solides dans les établissements multi-produits
- La réglementation biocide appliquée aux désinfectants utilisés dans l’Industrie Pharmaceutique : ce qu’il faut savoir…
- Cahier Pratique – Comment assurer le succès d’une auto-inspection du processus d’assurance de stérilité & des procédures associées
- La cryogénie est l’étude et la production des basses températures
- Stratégie de contrôle de nettoyage dans le cadre de la fabrication de Principes Actifs pharmaceutiques en développement à usage clinique
- Le contrôle visuel indirect modernise la validation du nettoyage
- La détermination du taux de recouvrement est une étape préliminaire, nécessaire lors d’un exercice de validation du nettoyage
- Cleaning Validation for biotechnological substances : What acceptance criteria ?
- “Health-based approach” implementation for setting limits in cleaning validation for Vaccines/Biotech
Lors de la production de lots de principes actifs pharmaceutiques commerciaux, une validation du nettoyage des installations dédiées est en général conduite. Les contrôles de nettoyage systématiques ne sont donc pas nécessaires. Dans le cas du développement de nouveaux actifs à usage pharmaceutique la problématique du nettoyage des installations doit être prise en compte dès la production des premiers lots à l’usage d’études cliniques des phases I à III.

Cet article décrit la stratégie appliquée au sein d’ORIL Industrie, groupe Servier, lors de la production de ces Nouvelles Entités Chimiques (NEC) engagées dans des études cliniques.
Les premiers lots de NEC sont en général fabriqués dans des ateliers nommés « multi-produits polyvalents». En effet, notre site fabrique simultanément des lots de principes actifs dans plusieurs indications, avec des niveaux d’avancement variés. Le taux d’attrition des produits en développement étant très important, aucune installation ne peut être dédiée avant la fin de la phase III. De nombreux actifs et intermédiaires se succèdent donc dans les installations. Le nombre de patients variant considérablement selon l’avancement des études et les indications, les tailles de batch, les types de réacteurs, sécheurs, broyeurs… sont très différents d’un lot à l’autre pour un même projet. Du fait de cette diversité, les croisements entre produits ne peuvent être anticipés mais le risque de contamination croisée doit être considéré dans le respect des Bonnes Pratiques de Fabrication.
Aucune validation de nettoyage ne peut être envisagée et les contrôles doivent donc être systématiques.
Une approche progressive
Le contrôle visuel est exigé à tous les stades de la synthèse. Il est effectué par les opérateurs et tracé dans les feuilles de marche sur des zones difficiles d’accès. Un démontage partiel ou complet du matériel est pratiqué afin d’appliquer un contrôle visuel efficace. Au besoin, un essuyage peut aider à l’examen visuel de zones difficilement accessibles.
Concernant les contrôles analytiques de nettoyage, une approche progressive est proposée basée sur une analyse de risque (1). Ainsi, le contrôle analytique de nettoyage est pratiqué en systématique sur le matériel utilisé pour la dernière étape chimique et la dernière étape physique de production de l’actif. Pour les étapes intermédiaires, le contrôle analytique est pratiqué pour les projets dont le niveau de développement est le plus avancé (phase II et III).
Les critères d’acceptation
La détermination du critère d’acceptation s’effectue à l’aide de toutes les données disponibles à l’instant sur ces produits. Un suivi en ligne des résultats des études de toxicologie et de pharmacologie est nécessaire pour s’assurer de leur prise en compte dans le calcul des critères d’acceptation. Des outils informatiques ont été développés afin de fiabiliser le stockage de ces informations. Plusieurs modes de calcul sont considérés systématiquement :
• Calcul à partir de la dose journalière d’administration,
• Calcul à partir de données toxicologiques : la PDE est prise en compte lorsqu’elle est disponible. En l’absence de cette donnée, les valeurs de DL50 peuvent être considérées. Le caractère génotoxique des composés est également pris en compte et un critère d’acceptation peut être calculé selon le Guideline ICH M7(2).
• Utilisation d’un critère dit chimique de 10 ppm de polluant résiduel dans le lot suivant.
• Après calcul de tous les critères possibles à partir des données disponibles, la valeur la plus basse est retenue pour l’acceptation du matériel.
La méthodologie de nettoyage
Avant la première transposition à l’atelier, des études en laboratoire sont menées afin d’acquérir des données de solubilité. Celles-ci sont utilisées pour mettre au point les premiers protocoles de nettoyage.
Ensuite, selon les expériences acquises lors des synthèses, les conditions de nettoyage peuvent être optimisées si besoin.
Prélèvement pour les analyses de contrôle de nettoyage
La plupart des contrôles analytiques de nettoyage sont effectués par rinçage surtout pour les réacteurs, filtres et isolateurs. Dès que cela est possible techniquement, un chauffage à reflux est effectué.Une analyse de risque menée sur le site autorise de ne pas réaliser de contrôles sur certaines petites pièces dont l’inspection visuelle est facile et dont la surface est très inférieure à celle du matériel principal. Le matériel est placé en quarantaine avant la réalisation du rinçage ou de l’essuyage. La quarantaine ne sera levée qu’après obtention d’une analyse conforme. Pour la dernière étape de traitement physique du principe actif, le contrôle prend en compte le train de matériels dans sa globalité.
Les techniques analytiques pour le contrôle du nettoyage
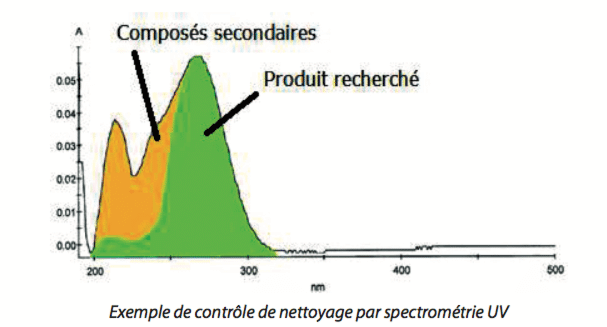
La plupart de nos NEC possèdent des groupements chromophores ce qui fait de l’UV une technique de détection de choix. La méthode développée il y a une dizaine d’année était non spécifique et consistait à réaliser le spectre UV du solvant de rinçage et à le soustraire du blanc de rinçage. Une quantification était ensuite réalisée à l’aide d’un spectre témoin du produit à rechercher. Le retour d’expérience pour cette méthode d’analyse non spécifique dans notre contexte est négatif : de très nombreux faux positifs étaient obtenus. Ceci était lié notamment à la topologie de l’atelier qui possède un système de doseurs de solvants pour alimenter les réacteurs. Ainsi une pollution du solvant de rinçage par 10 ppm d’un autre solvant possédant un chromophore très probable avec les doseurs de solvants industriels aboutissait à une non-conformité et à un nouveau nettoyage de l’installation alors que le contaminant n’est pas présent.
Pour améliorer la pertinence de nos contrôles, nous avons développé une méthode spécifique séparative. La chromatographie en phase liquide d’ultra-haute performance est le plus souvent utilisée pour sa précision et sa rapidité. La détection par UV à une longueur d’onde adaptée permet de doser les polluants potentiellement contenus dans le matériel. Cette technique permet de conserver une rapidité d’analyse puisque le résultat est obtenu en 15 min environ après la préparation de l’échantillon (chaque run dure 3,5 min). La phase stationnaire a été choisie pour retenir de façon optimale un maximum de composés. Le polluant est quantifié par étalonnage externe ou via un test aux limites. La sensibilité de la technique est adaptée aux critères d’acceptation de nos contrôles de nettoyage.
Les autres composés potentiellement présents sont également considérés et quantifiés au-dessus d’un certain seuil. Le contrôle de nettoyage peut être refusé en cas de teneur trop importante d’un composé inconnu. Les éluants ont été sélectionnés pour être compatibles avec un détecteur de masse. Ainsi en cas de nonconformité persistante, ce type de détection peut aider à comprendre l’origine du problème.
Voici un exemple d’apport de la spectrométrie de masse : ce contrôle de nettoyage était non conforme après plusieurs nettoyages et rinçages à cause de la présence d’un produit inconnu.
Grâce à la détection de masse, une hypothèse de structure a été émise pour ce polluant puis vérifiée à l’aide d’un étalon. La quantification de ce résidu couplée à l’analyse de risque réalisée par les opérationnels et l’assurance qualité a alors pu démontrer le faible impact pour la suite de la synthèse de l’actif. La quarantaine sur le matériel a pu être levée tout en assurant la sécurité des patients.
Pour chaque nouvelle recherche de polluant, lors du choix du solvant de rinçage, des éléments de validation sont effectués pour s’assurer de la pertinence de la méthode. Ce sont ainsi plus de 100 substances qui ont été recherchées avec succès depuis la mise au point de cette méthode.
D’autres méthodes alternatives telles que la Chromatographie sur Couche Mince (CCM) ou la Chromatographie en Phase Gazeuse (CPG) peuvent également être utilisées en cas d’absence de groupement chromophore. La méthodologie reste identique.
Conclusion
Le développement d’une méthode d’analyse spécifique permet à notre laboratoire de contrôle de réaliser plus de 150 analyses de contrôle de nettoyage par an pour la production de plusieurs dizaines de lots de principes actifs à usage clinique et d’assurer un risque maitrisé de contamination croisée.

Solenn JANVIER – SERVIER
solenn.janvier@servier.com
Partager l’article
Références
[1] Guidance on aspects of Cleaning Validation in Active Pharmaceutical Ingredient Plants Active Pharmaceutical Ingredients Committee (APIC) Sept 2016
[2] ICH Guideline M7 on assessment and control of DNA reactive (mutagenic) impurities in pharmaceuticals to limit potential carcinogenic risk Step 4