Sommaire
- ASTM E2500 : let's cross the Bridge !
- De l'étude du contexte à l'emploi de technologies de traitement des eaux adaptées
- Une nouvelle stratégie de gestion de l'eau en industrie pharmaceutique
- Cahier Pratique - Les boucles d'eau purifiée et la qualification. Focus sur la QP
- La mesure en continu dans l'eau à usage pharmaceutique (EUP)
- Candida auris, une espèce pathogène émergente "tueuse"
- Cleaning and disinfection program part of the lifecycle approach: a risk based rather arbitrarily imposed approach
- Eaux pharmaceutiques : les dessous de la maintenance des installations
- Pharma & the New Healthcare Economy. Ready or not ?
Les analyses dans l’eau à usage pharmaceutique s’inscrivent dans un contexte réglementaire, dicté par les pharmacopées et les guides de Bonnes Pratiques de Fabrication (BPF et GMP). Les fabricants d’instrumentation ont travaillé pour développer des analyseurs en ligne performants afin de suivre certains paramètres en continu. Ces instruments de mesure sont connus depuis de nombreuses années, ils ne sont pas toujours utilisés.

Ainsi, l’Annexe 15 des Bonnes Pratiques et le PAT (Process Analytic Technologie) vont dans le sens préférentiel de l’analyse en continu des paramètres clés, puisqu’ils permettent un suivi 24h/24h et augmente la réactivité en cas de dérive. Ces mesures permettent de valider en continu la qualité de l’eau à usage pharmaceutique dans les boucles de distribution.
Nous verrons les paramètres clés dans les boucles d’eau à usage pharmaceutique, et nous terminerons, en guise de conclusion sur l’aspect de l’eau destinée à la consommation humaine (eau potable) qui entre dans l’usine, car l’industrie pharmaceutique doit connaître et maîtriser la qualité de celle-ci. C’est effectivement un facteur déterminant dans la qualité de l’eau à usage pharmaceutique, et des traitements à mettre en œuvre.
1. Les paramètres clés
La conductivité
Pour résumer, il s’agit d’un indicateur, non spécifique, de pollution minérale (les ions) qui se traduit par la capacité de l’eau à conduire un courant électrique.
Le Carbone Organique Total (le COT)
C’est l’indicateur, non spécifique, d’une pollution organique. Nous pouvons définir le COT comme une source de nutriment des bactéries qui pourraient se développer dans les boucles d’eau à usage pharmaceutique (biofilm). Il s’agit de la matière organique issue du “vivant”. Parfois les contaminants proviennent de la décomposition de matériaux contenus dans les boucles de distribution d’eau à usage pharmaceutique. Effectivement le risque majeur est le développement de biofilm dans les boucles de distribution d’eau à usage pharmaceutique froide et surtout par rétro contamination. Certains points d’utilisation froids de boucles de distribution d’eau à usage pharmaceutique chaude peuvent être également contaminés.
L’ozone
Il s’agit d’un puissant oxydant utilisé pour la désinfection des boucles de distribution d’eau purifiée vrac froide, utilisée notamment pour la prévention de la contamination, et dans les cas extrêmes, pour détruire le biofilm.
2. Les principes de mesure
2.1 Principe de mesure de la conductivité
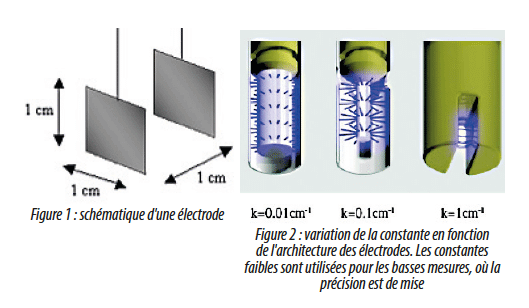
La mesure de conductivité est liée à la loi d’Ohm : U = R x I, U étant la tension en volts, R la résistance en ohms et I le courant en ampères. La conductivité C, exprimé en Siemens par centimètre est le résultat de l’équation suivante :
C = k x G, où G est l’inverse de la résistance exprimé en Siemens, et k, une constante exprimée en cm-1. Cette constante k est une valeur liée à la constitution de l’électrode de mesure : c’est le rapport entre la distance séparant les électrodes et leur surface : k = distance ÷ surface
La conductivité d’une solution dépend de :
- sa concentration ionique
- la valence des ions
- la nature de la solution (acide, basique ou neutre)
- la température.
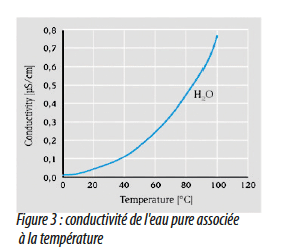
Ainsi, la conductivité, associée à la température traduit l’état de la minéralisation totale d’une eau. La courbe n’étant pas linéaire, il n’est pas suffisant d’introduire un coefficient de correction.
a) Application
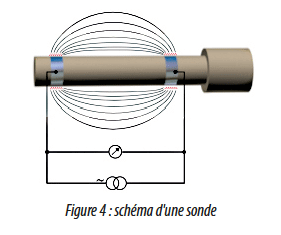
Dans la pratique, pour la mesure en ligne, les fabricants ont développés des capteurs constitués le plus souvent de 2 électrodes en matériaux nobles (acier inoxydable 316, titane, platine…) selon le principe vu précédemment :
Une tension alternative est appliquée aux électrodes en contact avec la solution à analyser. La conductance permet de calculer la conductivité, la concentration ou la résistance spécifique de la solution.
Cette technique est très efficace pour la mesure de faible conductivité. Dans les applications pharmaceutiques, la constante de cellule doit être certifiée, à +/- 2%. La résolution de mesure doit au moins être de 0,1 µS /cm. Et la mesure est toujours faite sans compensation en température, les pharmaciens préférant parler en valeur brute.
b) Vérification
Le contrôle de la constante de cellule peut se faire soit directement en mesurant avec le capteur une solution de conductivité certifiée (un standard étalon) ou indirectement, en comparant les résultats de l’analyseur (avec sa cellule) avec les résultats obtenus avec un analyseur dont la constante est certifiée. On parle d’analyseur “étalon secondaire”, lui-même rattaché à un étalon dit “maître”.
Le chapitre 645 de l’USP défini un test en 3 étapes (non décrit dans le présent article) pour s’assurer que la conductivité de l’eau respecte bien les limites de qualités.
La méthode indirecte, dans la pratique, est très facile à mettre en œuvre car on pourra certifier une cellule sans démonter le capteur en place, et permet de contrôler toute la chaîne en une fois (transmetteur, sonde et câble). Il est possible en effet de vérifier le transmetteur et le câble seuls, en utilisant des résistances de tests certifiées.
Dans la pratique, lorsque les vérifications sont erronées, le seul moyen qu’ont les pharmaciens est de jouer sur la constante de cellule, ce qui est pourtant, un non-sens par rapport au mot constante. Il faudrait remplacer le capteur qui dérive dans la logique, ou le nettoyer, car la seule justification à cette dérive est l’encrassement, ou dans le pire des cas, une modification intrinsèque de la géométrie par dégradation de l’électrode elle-même.
c) Où mesure-t-on ?
Les points de mesure en ligne sont les entrées et sorties du système de production de l’eau à usage pharmaceutique, et bien entendu les départs et retours de boucles.
2.2 Principe de mesure du Carbone Organique Total (COT)
Le principe de mesure du COT dans l’eau à usage pharmaceutique est indirect (boucles de distribution). Le COT est déduit de la soustraction du carbone inorganique (CIT) au carbone total (CT):
Pour différencier ces espèces du carbone, il va falloir décomposer le CT, afin d’obtenir la part de CIT.
Aujourd’hui nous trouvons sur le marché principalement les méthodes suivantes pour la détermination du COT:
- Oxydation thermique avec détection infra rouge (NDIR) (NON-DISPERSIVE INFRA RED)
- Oxydation couplée chimique et par radiation (persulfates et UV) avec détection NDIR, ou détection par la conductivité
- Oxydation UV directe avec détection de la conductivité
Oxydation
Dans les procédés d’oxydation thermique, les composants organiques se décomposent à une température élevée. Ainsi les composants non dissous (matières solides ou d’abrasion) peuvent être également complètement décomposés en CO2.
Dans les applications avec des charges organiques élevées (par exemple des eaux usées municipales) c’est une méthode éprouvée.
Dans les procédés d’oxydation couplée, les composants sont décomposés par un oxydant puissant, tel le persulfate, et également par une radiation UV. Cela permet un plus large champ d’utilisation [moins de 1 ppb (µg/L) à plus de 100 ppm (mg/L). En revanche, cela nécessite des produits chimiques de haute pureté et d’un gaz de purge, qui sont des facteurs de coût non négligeable.
Dans les procédés d’oxydation par lampe ultra violette, seule la radiation de la lampe est utilisée pour décomposer la matière carbonée. Cela implique une gamme de mesure plus faible et un échantillon de faible conductivité. Cependant, pour des applications en eaux pure et ultra pure, cette technique est très fiable et la moins onéreuse.
Détection
La détection NDIR : Il s’agit d’un détecteur infrarouge qui mesure le CO2 généré en déterminant la quantité de lumière infrarouge absorbée par le CO2 à une distance connue.
La détection par sonde de conductivité : le CO2 généré va impacter la conductivité en augmentant sa valeur. Le calcul se fait à l’aide de tables de conversion connues.
Dans l’industrie pharmaceutique, la réglementation est fixée par les pharmacopées :
- Pharmacopée américaine, COT : USP 643,
- Pharmacopée européenne, COT : EP 2.24,
- Pharmacopée japonaise, JP,
Le COT étant un nutriment des bactéries, il va de soi que l’eau à usage pharmaceutique qui entre dans la composition des médicaments doit être exempte de COT, pour empêcher leur prolifération et le développement de biofilm.
a) Application : Méthode UV/différentiel de conductivité pour le contrôle d’une boucle d’eau purifiée
Dans ce procédé, l’analyseur en ligne va aspirer l’échantillon de la boucle. Après la première mesure de la conductivité, l’échantillon entre dans un réacteur UV. A l’intérieur, le carbone organique présent dans l’eau à usage pharmaceutique est oxydé en CO2. Ce CO2 à son tour augmente la conductivité mesurée. Cette conductivité est mesurée après un second capteur placé après le réacteur UV.
La différence entre la seconde et la première mesure de conductivité, il est possible de calculer le COT sur le principe suivant :
Cette méthode reconnue est la plus simple et la plus rapide. Le temps de réponse est inférieur à 2 minutes. La surveillance du processus est continue ce qui permet de mieux maîtriser sa boucle de distribution d’eau à usage pharmaceutique. Il est intéressant de choisir ce type d’équipement, car les coûts d’investissement, de fonctionnement et d’exploitation sont très intéressants.
Le domaine d’application de ce principe de fonctionnement est intéressant que pour les eaux pures et ultra pures dont la conductivité est inférieure à 2 µS/cm à 20° C. Ce principe de mesure est très adaptée à l’eau à usage pharmaceutique. La différence entre le CT et le CIT est conséquente. Le CIT n’est pas très élevé et essentiellement du CO2, ce qui permet d’avoir des résultats fiables sur la gamme 0 à 1000 ppb.
b) Vérification
Les monographies définissent également les critères pour l’étalonnage de la mesure. Cet article ne décrit pas toutes les modalités, pour la fabrication des solutions certifiées d’étalonnage et de validation de la mesure :
- le matériel doit être étalonné : à l’aide d’une solution étalon
- la limite de détection doit être inférieure à 50 ppb
- la détermination du COT doit se faire par la soustraction du CIT au CT
- un paramètre fondamental : le SST (“System Suitability Test” doit être effectué tous les 6 mois)
Ce test permet de vérifier que l’analyseur est capable d’oxyder aussi bien des liaisons simples que complexes :
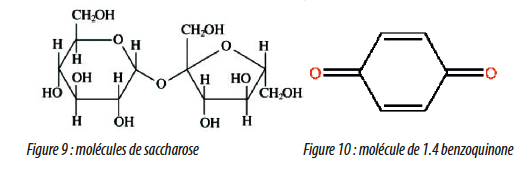
Pour faire le SST, nous allons utiliser des solutions de saccarose (liai- sons simple) et de 1,4 benzoquinone (liaisons complexes) donnant des réponses en COT = 500 ppb +/- 15 %. L’eau qui a servi à préparer ces solutions est appelé blanc.
Le succès du test est exprimé en efficacité relative :
- Réponse du blanc de l’eau rw = < 100 ppb COT
- Réponse de la solution étalon 1 rs: sucrose RS à 500 ppb COT
- Réponse de la solution étalon 2 rss: 1,4-benzoquinone RS à 500ppb COT
Le test est réussi si le résultat est compris entre 85 et 115 %. Nous nous assurons ainsi de la conformité de l’analyseur et il est ainsi validé.
Dans la pratique, ce test est fait tous les 6 mois, période où la maintenance est également effectuée.
- Réalisation du SST pour s’assurer que les 6 mois précédents sont bien valides
- Réalisation de la maintenance, remplacement de pièces préconisées, comme par exemple, une lampe UV,
- Réalisation d’un étalonnage sur la pleine échelle de l’analyseur (facultative mais conseillée)
- Réalisation du SST pour validation et départ des 6 mois
c) Où mesure-t-on ?
Les points caractéristiques à suivre sont :
- le retour de boucle de distribution d’eau à usage pharmaceutique
- il peut-être recommandé de faire des mesure en sortie des distillateurs
- mais surtout en sortie de résine échangeuse d’ions.
2.3 Principe de la mesure d’ozone
Rappel USP- NF 24<1231>
“Les agents chimiques stérilisants devant être utilisés dans les boucles d’eau à usage pharmaceutique et destinés au contrôle des micro-orga- nismes doivent être du chlore ou de l’ozone…Ces substances ne sont pas considérés comme des substances additionnelles aussi longtemps qu’elles sont éliminées tout au long du déroulement du procédé ou bien absente de l’eau pure. Le contrôle de ces agents doit garantir une concentration constante et donc permettre leur surveillance pour garantir qu’ils ne sont plus présents.”
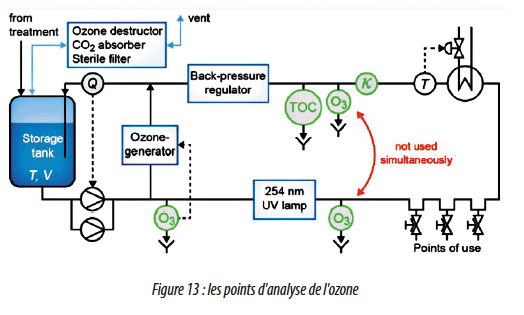
L’analyseur d’ozone en continu contrôle :
- la quantité d’ozone introduit à l’entrée du générateur d’UV
- la non présence d’ozone en sortie du générateur UV (UV en fonction)
- la mesure de la quantité d’ozone en retour de boucle de distribution (UV à l’arrêt).
Les principes de mesure sont la méthode électrochimique et la méthode spectrophotométrique.
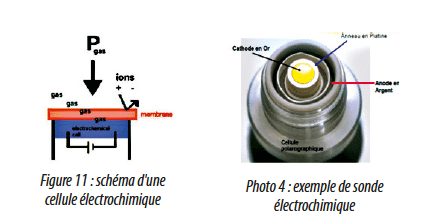
a) Principe / méthode sonde ampérométrique
La première technique utilise des capteurs ampérométriques fonctionnant sur le principe suivant :
- le gaz se dissout et diffuse à travers la membrane puis l’électrolyte
- réaction de réduction sur la cathode = production d’ions
- le courant induit est proportionnel à la concentration en O3
La sensibilité de la sonde ampérométrique (électrochimique) est bonne. S’il n’y a pas de courant induit, il n’y pas d’ozone. L’inconvénient majeur de cette technologie est le phénomène de polarisation et de dépolarisation.
En effet, il faut une présence régulière d’ozone pour polariser le capteur. La mesure électrochimique (sonde ampérométrique) présente un inconvénient majeur de fiabilité concernant la mesure d’absence d’ozone. Le capteur se dépolarise rapidement et il faut constamment lui faire “voir” de l’ozone, ce qui implique des systèmes d’automatismes avec des coûts associés.
Le fait de mesurer de faibles valeurs en ozone avec ce type de capteur impacte fortement les temps de réponse qui sont allongés.
Un inconvénient supplémentaire est celui de la maintenance (remplacement de la membrane), qui oblige l’interruption de la mesure, une procédure d’étalonnage et de polarisation qui prend du temps (parfois jusqu’à 4 jours).
b) Vérification pour les méthodes ampérométriques
Le zéro est établi à l’air, (ainsi qu’un contrôle de la pression et de la température), utilisant le principe du rapport O2/O3 supposé constant. Ensuite, l’ozoneur est mis en marche forcée pour atteindre une valeur d’au moins 100 ppb, contrôlé avec une méthode de référence. La méthode de référence est la spectrophotométrie.
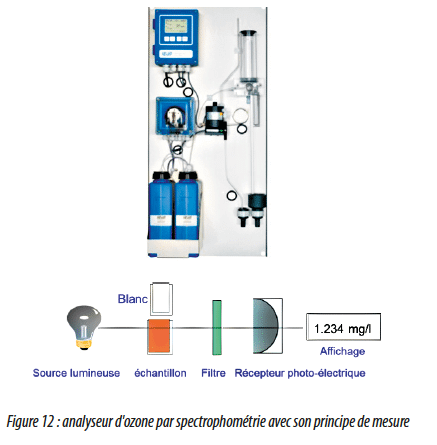
c) Principe/ méthode de mesure spectrophotométrique
Tous les précédents inconvénients sont gommés en utilisant directement l’analyseur en ligne par spectrophotométrie.
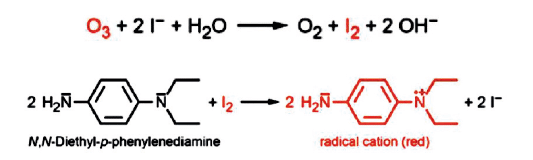
Cette méthode est la méthode de référence normalisée pour la mesure de l’ozone, à la DPD-IODURE, selon DIN-38408-3.
En présence d’ozone, un ajout de ces réactifs dans l’échantillon provoque une coloration qui est lue grâce au spectrophotomètre. Cette intensité de coloration est directement proportionnelle à la concentration en ozone.
Pas de coloration = 0 ozone et la précision est de 1 ppb.
L’inconvénient de cette méthode est qu’elle utilise des réactifs spécifiques, mais garanti une mesure d’ozone beaucoup plus fiable et surtout dans une garantie de la mesure d’absence, car il n’y a pas de dépolarisation.
d) Vérification pour les méthodes spectrophotométrique
La métrologie est beaucoup plus facile car il suffit de placer des étalons secondaires dans le photomètre pour calibrer la pleine échelle, un point en basse gamme et le zéro est réalisé avant chaque mesure.
Cet instrument ne présente pas de perte de temps après une maintenance car les phénomènes de polarisations sont absents. La mesure est fiable dès la première mesure.
Il faut toutefois préciser un point essentiel pour la mesure d’ozone :
Echantillonnage de l’eau
- l’eau doit être en mouvement
- éviter les points de dégazage :
- aspiration d’une pompe ou après une vanne
- au niveau d’un coude ou d’un point bas
- au sommet d’une canalisation horizontale
- canalisation verticale
Il n’y a pas de réglementation sur les analyses d’ozone mais des recommandations :
- recommandation ISPE pour la désinfection (20ppb < O3 < 200 ppb).
- recommandation SWAN (10 ppb < O3 < 30 ppb).
- la mesure d’ozone en sortie générateur d’UV est comprise entre 0 ppb et 5 ppb.
e) Où mesure-ton ?
Conclusion
Les mesures en continu de ces différents paramètres sont des atouts qualitatifs et économiques. Ces mesures garantissent en continu la qualité de l’eau à usage pharmaceutique et permet une plus grande réactivité.
Lorsque nous connaissons le coût associé des non- conformités, et du temps qu’il faut pour les traiter, il est incontestable que ces systèmes d’analyses en ligne sont aujourd’hui essentiels dans la conduite des installations.
Nous vous rappelons que l’eau potable (destinée à la consommation humaine) entrant sur le site est de la responsabilité du site. Nous pouvons déjà considérer que l’eau potable est une eau à usage pharmaceutique puisqu’elle alimente tout le site.
Le site doit faire réaliser des analyses régulières par des laboratoires agréés et doit contrôler quelques paramètres :
- Mesurer le chlore à l’entrée de l’usine est important pour savoir si le risque de contamination est maîtrisé en amont, mais aussi pour dimensionner les systèmes d’élimination de chlore en aval. Le chlore est à éliminer pour protéger les membranes d’osmose inverse et les systèmes d’électro-déionisation qui sont dégradés par le chlore résiduel.
- Installer un analyseur d’absence de chlore total avant les membranes est un atout économique, lorsque nous connaissons le coût des membranes d’osmose inverse et surtout les systèmes d’électro-déionisation.
- La turbidité (bien qu’elle ne soit pas l’indice réel de colmatage de l’eau) peut être un bon indicateur pour éviter un colmatage des membranes d’osmose inverse lors d’une dérive à la hausse de la turbidité.
- La conductivité est un indicateur de la charge ionique d’eau potable.
- La dureté peut être également à suivre en fonction du traitement de potabilisation.

Benjamin GRACIA – SWAN
Formé aux métiers de l’eau ainsi qu’aux composantes afférentes comme l’électrotechnique et les infrastructures en génie civil, il commence son activité dans l’industrie, pendant plus de 5 ans, chez Suez et OTV, dans divers services d’exploitation et de conduite de travaux. Il a été confronté à un certains de nombre de problématiques lié à la qualité de l’eau et à l’importance des outils analytiques. Dès 2010, il rejoint Swan France Instruments d’analyse, en tant que chargé d’affaires pour puis responsable Grands Comptes. Il participe activement dans ce cadre au développement du marché pharmaceutique.
benjamin.gracia@swan-france.fr
Partager l’article
Bibliographie
USP<643> “Total Organic Carbon”, United States Pharmacopoeia 36-NF 31, U.S. Pharmacopeial Convention Inc., Rockville, Md. (2013).
USP<645> “Water Conductivity”, United States Pharmacopoeia 36-NF 31, U.S. Pharmacopeial Convention Inc., Rockville, Md. (2013).
USP<1231> “Water for Pharmaceutical Purposes”, United States Pharmacopoeia 36-NF 31, U.S. Pharmacopeial Convention Inc., Rockville, Md. (2013).
EP 2.2.38 “Conductivity”, European Pharmacopoeia, vol. 7.0, Council of Europe, Strasbourg, France (2013).
EP 2.2.44 “Total Organic Carbon in Water for Pharmaceutical Use”, European Pharmacopoeia, vol. 7.0, Council of Europe, Strasbourg, France (2013).
Guides ISPE (International Society for Pharmaceutical Engineering)
Annexe 15 du Guide Communautaire des Bonnes Pratiques
Glossaire
EPV : eau purifiee vrac
EPPIV : eau pour préparation injectable vrac